9. A ativação das moléculas de um certo tipo depende da quantidade de colisões entre as moléculas. Seja a(t) a quantidade de moléculas não-ativadas por unidade de volume, e b(t) a de moléculas ativadas. A ativação depende da colisão entre moléculas não-ativadas, logo ela é proporcional a a²(t); a desativação envolve colisões entre moléculas ativadas e não-ativadas, sendo proporcional a a(t)b(t). As equações abaixo representam tal modelagem:
Utilizando a(0) = 1, b(0) = 0, k = 0,2 e r = 0,1, investigue o que ocorre quando d = 0 e d = 0,1.
Utilizando-se o método de Runge-Kutta de 4ª ordem, com h = 0,1, verifica-se que as quantidades a e b tendem a se estabilizar quando d = 0, com a(100)≅ 0,3333 e b(100)≅ 0,6666. Já quando d = 0,1, obtemos a(400)≅ 0,0133e b(400)≅ 0,0003, sem que as mesmas se estabilizem.
Utilizando a(0) = 1, b(0) = 0, k = 0,2 e r = 0,1, investigue o que ocorre quando d = 0 e d = 0,1.
Utilizando-se o método de Runge-Kutta de 4ª ordem, com h = 0,1, verifica-se que as quantidades a e b tendem a se estabilizar quando d = 0, com a(100)≅ 0,3333 e b(100)≅ 0,6666. Já quando d = 0,1, obtemos a(400)≅ 0,0133e b(400)≅ 0,0003, sem que as mesmas se estabilizem.
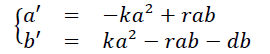
Nenhum comentário:
Postar um comentário